Anlage 1: Checkliste um die Schimmelpilzentstehung zu vermeiden
- Überprüfung der Lüftungsgewohnheiten, Querlüftung 3-4 Mal täglich, 5-15 Minuten lang;
- Kontrolle der Raumlufttemperatur, die Differenz innerhalb einer Wohnung sollte etwa 4 K nicht überschreiten, dabei sind die Raumtemperatur und die Temperatur in der kühlsten Raumecke möglichst über den Fußboden zu messen. Als Hilfsmittel steht das Berechnungstool unter www.ib-rauch.de/Beratung/schim/feucht1.php zur Verfügung.
- Erhöhtes Feuchtigkeitsaufkommen beim Backen, Braten, Kochen, Duschen, Baden sofort direkt ins Freie ableiten. Keine Verteilung der Feuchtigkeit in der Wohnung durch geöffnete Türen zu lassen.
- Einsatz technischer Hilfsmittel (Entlüftungseinrichtung oder Lüftungsleisten)
- Messung der Feuchtigkeit mit einem Hygrometer, eine relative Luftfeuchtigkeit von ca. 60 % sollte als Obergrenze eingehalten werden. Besser sind Werte um 50 % besonders im Winter.
- Einrichtungsgegenstände an Außenwänden sind nicht luftstrombehindernd anzuordnen (mind. 5 cm Abstand zur Wand). Raumecken sind möglichst frei zuhalten.
- Prüfung des Standortes des Heizkörpers. Kann eine richtige Luftwalze entstehen und werden durch diese alle Außenwandteile ausreichend erfasst.
- Verwendung diffusionsoffener Baustoffe, Vermeidung von Dampfbremsen und Austrocknung feuchter Bauteile vor jeder Sanierung!
- Nachträgliche, zusätzliche Dämmmaßnahmen immer so anordnen, dass die Dämmschicht möglichst weit außen liegt, also dort, wo der Wärmeverlust am größten ist.
Anlage 2: Ausgewählte Toxine - eine Zusammenstellung aus verschiedenen Literaturquellen
Aflatoxine
Gruppe von Stoffwechselprodukten der Schimmelpilze Aspergillus flavus, A. parasiticusu. a., die bestimmte Nüsse, Mais u. Getreidemehle befallen. A. zählen zu den gefährlichsten
Pilzgiften (Mycotoxinen) und stärksten Lebercarcinogenen 1.2. Bekannt wurden sie als Verursacher des Truthahnsterbens, dem 1960 in Großbritannien 100.000 Truthühner zum Opfer fielen 3.
Tab.: Aflatoxine.
| Aflatoxine | Summenformel | MR | Schmp. [°C] | Drehwert (a]D | CAS |
| B1 | C17H12O6 | 312.28 | 268 - 269 | -562° (CHCl3) | 1162-65-8 |
| B2 | C17H1406 | 314.29 | 305 | -492°(CHCl3) | 7220-81-7 |
| B2a | C17H1407 | 330,29 | 217 | 117878-54-5 | |
| P1 | C16H1606 | 298,25 | >320 | -574° (CH3OH) | 3225-02-4 |
| B3 | C16H1406 | 302,28 | 217 | 23315-33-5 | |
| G1 | C17H1207 | 328,28 | 247- 250 | -556° (CHCl3) | 1165-39-5 |
| G2 | C17H1407 | 330,29 | 237- 240 | -473° (CHCl3) | 7241-98-7 |
| G 2a | C17H1207 | 328,28 | 299 | -280° (DMF) | 6795-23-9 |
| M 2 | C17H1407 | 330,29 | 293 | 6885-57-0 | |
| GM1 | C17H1208 | 344,28 | >276 | 23532-00-5 | |
| GM2 | C17H1406 | 346,29 | 270- 272 | ||
| Q1 | C17H1207 | 328,28 | 266 |
|
52819-96-2 |
A. flavus bildet die A. B1 u. B2; A. parasiticus zusätzlich noch G1 u. G2 (B = blau u. G = grün stehen für die Fluoreszenz im UV-Licht). Andere A. sind tierische oder mikrobielle Stoffwechselprodukte dieser vier (z.B. M1, M 2, GM2, P1, Q1). Verbindung. der M-Reihe treten besonders in der Milch u. Milchprodukten auf. Die A. bestehen alle aus einem Dihydrofurofuran- bzw. Tetrahydrofurofuran-Ringsystem, das an ein substituiertes Cumarin-System ankondensiert ist.
A. sind die einzigen Toxine, deren max. Gehalt in Lebens- u. Futtermitteln gesetzlich geregelt ist5 (Aflatoxin-Verordnung). Für den Nachweis im pgng Bereich sind Antikörper für ELISA-Tests erhältlich.
Aflatoxin B1 ist das am häufigsten vorkommende, am stärksten toxisch u. carcinogene Aflatoxin. Die Giftigkeit der A. hängt einmal von der Struktur, zum anderen aber von den individuellen Voraussetzungen des einzelnen Organismus bzw. Zelltyps ab. Primär wird die Leber angegriffen, aber auch Nierenschädigungen treten auf. A. B1 wird durch mikrosomale Enzyme metabol. aktiviert, dabei entsteht ein reaktives Epoxid. Dieses kann sowohl an DNA als auch chromosomale Proteine binden. Die mutagene u. carcinogene Wirkung wird durch eine kovalente Bindung an N-7 eines Guanosins der DNA mit anschließenden Folgereaktionen u. dadurch bedingte Mutation im Gen p53, einem Tumorsuppressor-Gen. erklärt. In Hepatozyten kommt es in Gegenwart von A. B1 zu einer G --> T Umwandlung, die zu einem Austausch von Arginin durch Serin im codierten Protein führt. Diese G --> T Umwandlung findet man auch in Lebertumoren6. A. B1 u. Hepatitis B Virus wirken synergist. in der Leber7. Bes. empfindlich auf A. B1 reagieren Forellen u. Entenküken (LD50 18 µg/50 g Körpergewicht). Die Biosyntheseschritte sind incl. der beteiligten Enzyme u. z.T. der Gene aufgeklärt7. - E aflatoxins
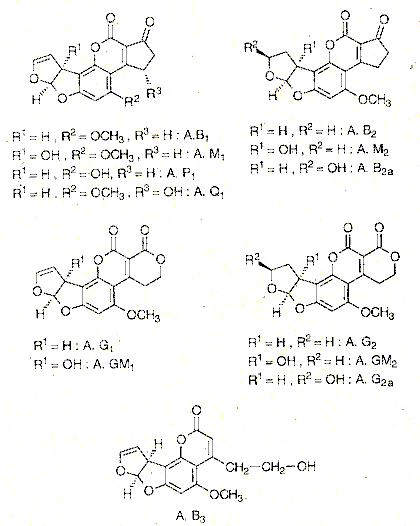
Lit.: Nature (London) 267. 863 (1977).2 Proc. Natt. Acad. Sei USA 80, 2695-2698 (1983).3
Endeavour 1963.75-79.4 J. Am. Chem.Soc.85,1705(1963);87,882(1965) 5 BGBl. I. S. 3313 i.d.F. der Änderungs-VO vom 6.11.1991.6 Nature (London) 350, 427-428, 429-432 (1991).7 Handbook of Applied Mycology. Bd. 5, Mycotoxins in Ecological Systems. Kapitel 10 u. lt. New York: Marcet Dekker 1992: Appl. Environ. Microbiot. 59, 3273-3279 (1993): Lancet 339. 943 964 (1992).
allg.: Angew. Chem. 96. 462-474 (1984) - Betina. Kapitel 7. Cote-Cox, 5. 1-66. - Biosvnth.: Microbiot. Re,. 52. 274-295 (1988). Biochemistry 30.4343-435(1(19911 . Appt. Environ. Microbiol. 59. 3564-3571 (1993). - Carcinogenese: Proc. Natl. Acad. Sci USA 83, 9418-9422 1986): 90, 8586-8590 (1993) - J. BioI. Chem. 264. 12226-1231 (1989). -Epidemiologie: Annu. Rev. Phytopathot. 25. 249-270 (1987).
- Svnth.: J. Org. Chem. 51. 1006 (1986) - Sax 18.). AET-AEW 500. Synthesis 1988. 760. [HS 2932 90] [172]
Aflatrem (a,a-Dimethylallylpaspalinin)
a,a-Dimethylallylpaspalinin C3H39NO4, MR 501,67, Nadeln, Schmelzpunkt 222-224 °C, Inhaltsstoff von Aspergillus flavus - Sklerotien u. Mycel, gehört zu den tremogenen Toxinen, welche bei Tieren Zittern u. Krämpfe hervorrufen (s.a. Paspalin bei Paspalitreme). In den Sklerotien wird A. Schutzfunktion vor Tierfraß zugeschrieben. - E aflatrem.
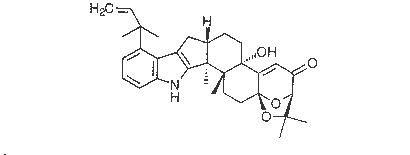
Lit.: - Cole-Cox. S. 410-413, - Science 44, 177 (1964), - Tetrahedron Lett. 1980. 239. - [CAS 70553-75-2] [174]
Fumitremorgene
Gruppe neurotox. 6-Methoxyindol-Alkaloide aus Aspergillus- u. Penicillium-Arten. Lanosulin, das von Penicillium lanosum gebildet wird, ist identisch mit F. B. Die F. zählen zu den Mycotoxinen die tremorgene Effekte auf Tiere haben (=Zittern auslösen). Andere Verb. mit dieser Eigenschaft
sind z. B. die Aflatreme, Janthitreme, Penitreme (Tremortine), Paspalitreme, Territreme u. Verrucosidin.
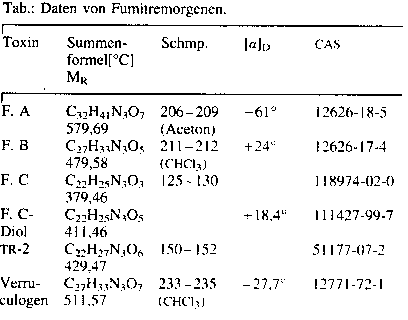
Mit Ausnahme der Territreme u. des Verrucosidins leiten sich alle biosynthetisch von Tryptophan ab. F. A u. B. rufen in Dosen von 1 mg/Tier (i.p.) bei Mäusen Tumor hervor, 5 mg/Tier führen in 70% zum Tode. Verruculogen führt bereits bei 0,01 mg/Tier zu Zittern. Insbesondere Weidetiere sind von diesen Toxinen betroffen (s. Taumellolch). Penicillium piscarium, von Gras isoliert, produziert Verruculogen u. F. B.; A spergillus fumigatus aus verschimmelten Mais-Silagen produziert Verruculogen. F. A, F. B u. TR-2. — E fumitremorgins.
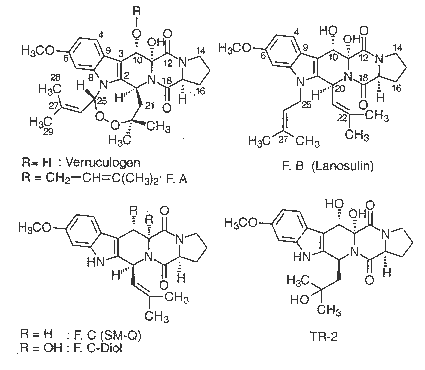
Lit.: Betina. Kapitel 16 - Chem. Pharm. Bull. 37. 23—32 (1989) CoIe-Cox. S. 335—509 - Steyn u. Vleggar. Mycotoxins and Phycotoxins. S. 399—408, 501 —512. Amsterdam: Elsevier 1986 - Steyn (Hrsg.). The Biosynthesis of Mycotoxins. S. 204—209. New York: Academic Press 1980 - Tetrahedron 44. 359—377. 1991—N)00 (1988): 45, 1941 (1989) - Tetrahedron Lett. 28. 1131 (1987): 29, 1323 (1988) - Turner 2.410—413. 535ff. - Zechmeister 48.54—60. [175]
Mycotoxine
Niedere Pilzmetabolite, die in Nahrungs- und Futtermitteln vorkommen und bei Menschen und Tiere Symptome einer Mycotoxicose (Z. B. Sankt Antonius-Feuer, Ergotismus, Kashin Beck-Krankheit) hervorrufen. Werden M.-haltige Futtermittel an Schlachttiere verfüttert, können M. auch in Eiern, Fleisch oder Milch auftreten, man spricht dann von "carry-over". Teilweise wirken M. auch gegen andere Mikroorganismen, sodass die Abgrenzung zu den Antibiotika nicht immer eindeutig ist. Zu den am stärksten befallenen Lebensmitteln gehören Getreide u. -erzeugnisse, Nüsse, Erdnussbutter, Presskuchen von Ölpflanzen (in die Öle gehen meist nur <10% der Toxine über), Reis, Mais, Malz, Fruchtsäfte (insbes. Apfelsaft), Milch u. Käse. M. Produzenten sind v. a. Aspergillus-. Penicillium-, Fusarium-, Claviceps-(Ergot-Alkaloide) und Rhizopus-Arten. M. können bereits auf dem Feld oder erst bei der Lagerung (auch im Kühlschrank) gebildet werden. Bekannte M. sind die Aflatoxine (die stärksten natürlichen
Carcinogene), Byssochlamsäure, Citrinin, Citreoviridine, Fumonisine, Patulin, Ochratoxine, Sterigmatocystin, Ergot-Al-kaloide, Ergochrome, Cytochalasin, Penicillsäure, Zearalenon, Penitreme, Trichothecene u. andere.
Den sichersten Schutz vor Mycotoxinvergiftungen bietet das Vermeiden des Verzehrs von verschimmelten Lebensmitteln. Pflanzenschutz- u. Konservierungsmittel verhindern Schimmelpilzbefall.
Für einige Mycotoxine gibt es gesetzlich festgelegte Höchstmengen. z. B. ist der max, zulässige Aflatoxin-Gehalt von Lebensmitteln in 60 Ländern geregelt. Die Grenzwerte in den einzelnen Ländern schwanken
zwischen 0.05 u. 5 g/kg. In jüngerer Zeit sind M. vom Trichothecen-Typ als Kampfstoffe in Verruf gekommen.1
Lit.: 1 Nachr. Chem. Tech. 32.598 (1984): Nature (London) 309. 207 (1984). aIlg.: Chem. lnd. (London) 1995. - Dtsch. Tierärztl. Wochenschr. 96. 346. 355 (1989) - Food Rev. Int. 6. 115 (1990) - Fördergemeinschaft Integrierter Pflanzenbau (Hrsg.). - Natürliche Gifte in Getreide. Bonn: Rheinischer Landwirtschafts-Verl. 1990 - Forum Mikrobiol. 138 (1981) - Reiß (Hrsg.). Mykotoxine in Lebensmitteln. Stuttgart: G. Fischer 1981, - Reiß, Schimmelpilze — Lebensweise. Nutzen. Schaden. Bekämpfung. Berlin: Springer 1986 - Rev. Environ. Contam. Toxicol. 127, 69-94(1992) - Samson u. van Reenen-Hoekstra, lntroduction to Food-borne Fungi. Baarn: CBS 1988. [176]
Paspalitreme
Gruppe tremorgener Mycotoxine aus Claviceps paspali, Aspergillus flavus A. nomius. Die Verbindungen werden in Submerskulturen gebildet, kommen aber auch in Sklerotien der Pilze vor, wo man ihnen eine Schutzfunktion gegen Insektenfraß zuschreibt. Daneben findet man diese Neurotoxine auch bei Befall durch Claviceps paspali in Weidegras (Paspalum dilatatum), wo es zu "paspalum staggers" (s. Taumellolch) bei Weidetieren führt. Man unterscheidet die P. A. B u. C, Paspalin, Paspalinin sowie Paspalicin, z. B. P. A, C32H39N04, MR 501,67, amorph; Paspalin, C28H39NO2, MR 421,62, Schmp. 264 °C; Paspalicin, C27H31NO3, MR 417,55, Schmp. 230 - 240 °C. A. nomius bildet 14-Hydroxypaspalinin u. 14-(N,N-Dimethyl-L-valyloxy) paspalinin. - E paspalitrems
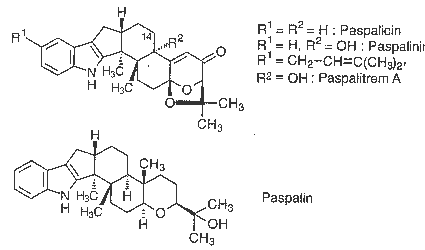
Lit.: Betina. S. 366-371 - CoIe-Cox. S.390-409 - J. Agric. Food Chem. 25. 826. 1197 (1977); 29, 293 (1981); 32. 1069 (1984).Tetrahedron Lett. 21, 231. 235 (1980); 34, 2569 (1993); - Zechmeister 48. 32—45 - s.a. Janthitreme u. Penitreme. - [CAS 63722-90-7 (P. A): 11024-56-9 (Paspalin); 11024-55-8 (Paspalicin)] [177]
Territreme
Gruppe von tremorgenen Mycotoxinen, die von Aspergillus terreus gebildet werden. Im Gegensatz zu den Penitremen Aflatrem und anderen Tremorgenen enthalten die T. keinen Stickstoff. - E. Erritrems
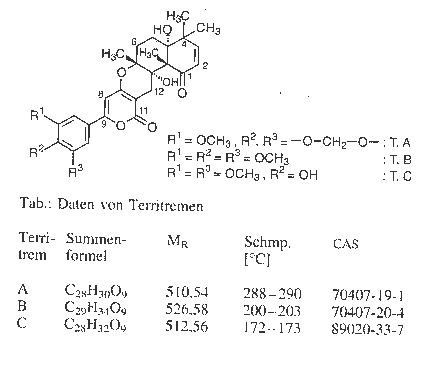
Lit.: Appl. Environ. Microbiol. 37. 355, 358 (1979); 47. 98 (1984) 54. 585 (1988; - J. Nat. Prod. 55. 251 (1992); - Zechmeister 48. 45-48 [178]
Verrucosidin
C24H32O6 MR 416.51. Schmp. 90-91 °C . [a]D +92,4 (CH3OH) tremorgenes Mycotoxin, das von Penicillium verrucosum var. cyclopium und anderen Penicillium-Arten gebildet wird. V. ist strukturell verwandt mit den Citreoviridinen und Asteltoxin. E verrucosidin.
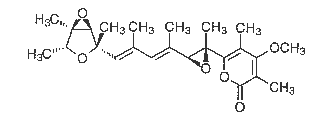
Lit.: J. Am. Chern. Soc. 112. 8985 (1990); - J. Org. Chem. 59 3762 (1964); - Zechmeister 48. 49 f. [CAS 88389-71-3] [179]
Verrucolotoxin.
C 15H20N2O. MR 244.34. Schm 152 °C, [a]D -56 °(CH3ON); tremorgenes Mycotoxin aus grünen Erdnüssen, die mit Penicillium verrucosum infiziert sind. Die LD50 Werte für Küken liegen bei 20mg/kg, die Tiere sterben innerhalb von 4-6 Std. nach Verabreichung. [179]
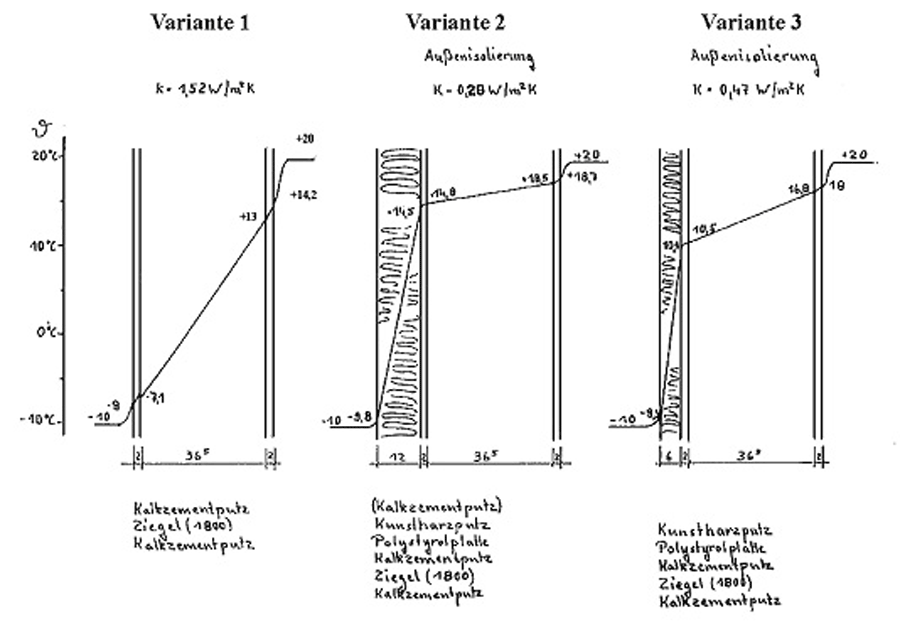
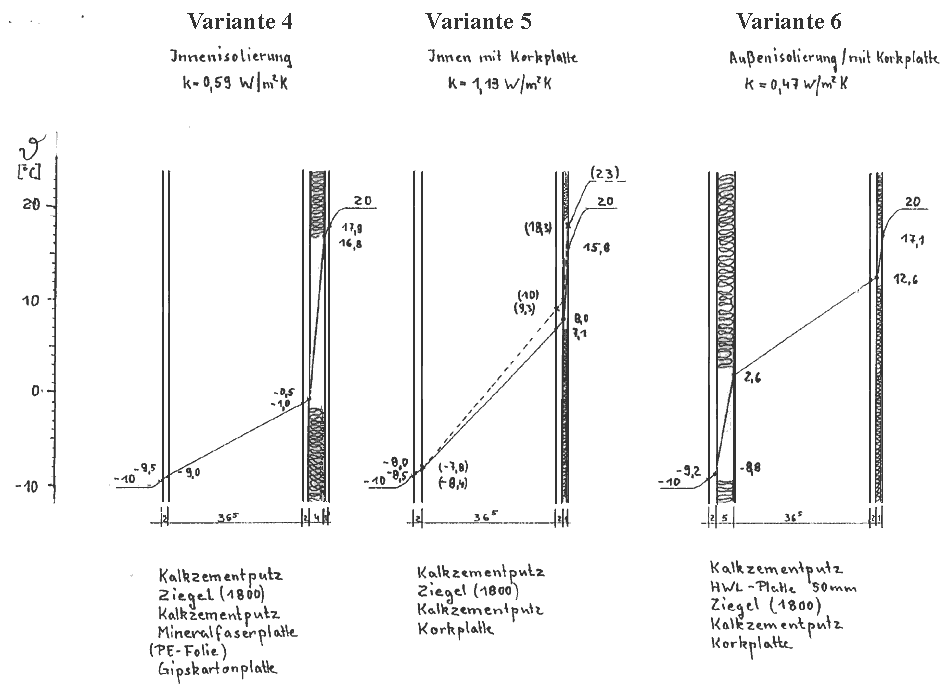
Anlage 3: Innen- und Außendämmung bei einer Außenwand
Eine 36,5er Ziegelwand wird mit unterschiedlichen Dämmstoffen als Außen- oder Innendämmung versehen. Hier wird der theoretische Temperaturverlauf im Wandquerschnitt und an der Innenseite dargestellt. Bei der Variante 1 und 5 besteht eine Gefährdung an der Innenwandoberfläche durch Schimmelpilzbildung. [180] Die praktische Oberflächentemperatur an einer Fassade mit Wärmedämmung ist, ausgenommen bei Sonnenschein, niedriger als die der Außenlufttemperatur.
Anlage 4: Luftfeuchte und Taupunkttemperatur [74]
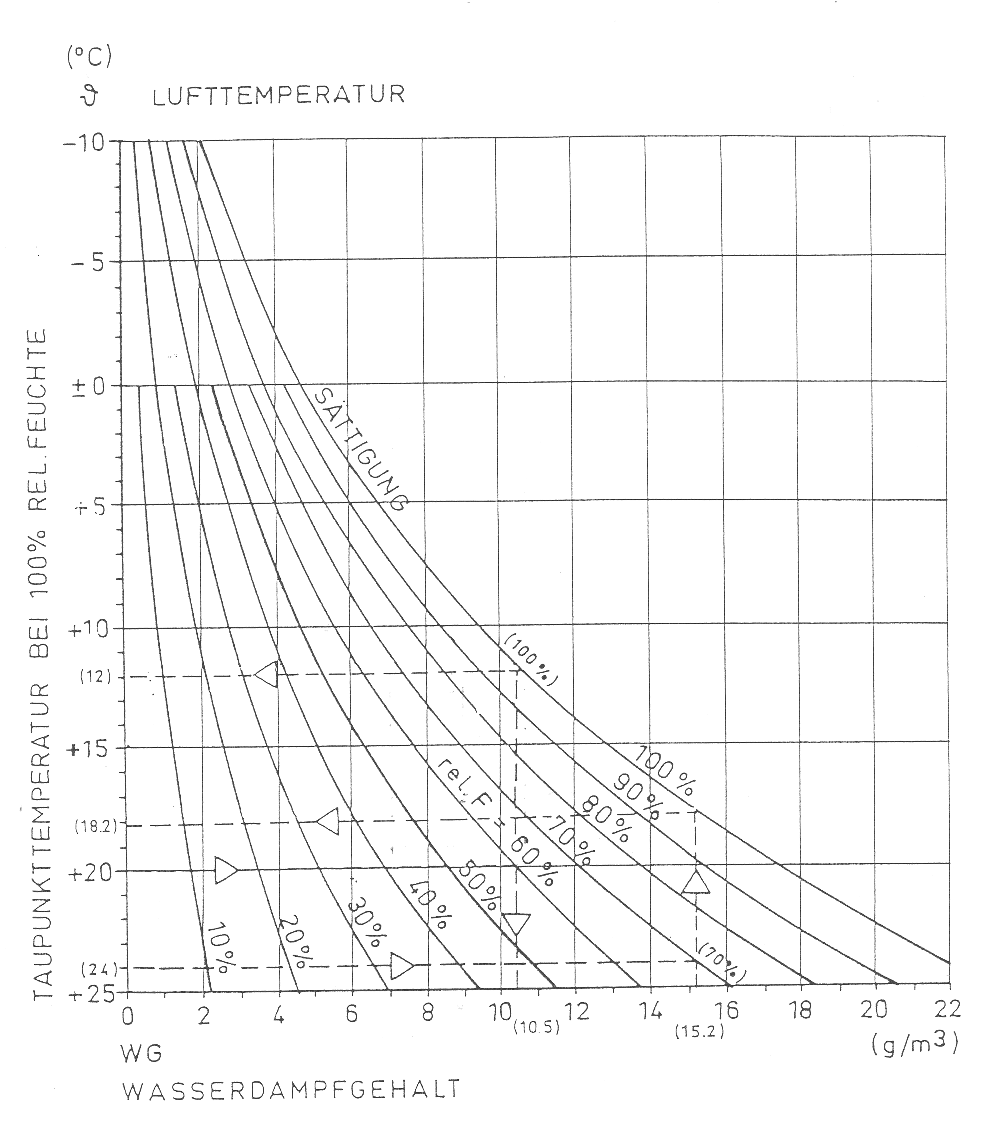
Beispiel zur Erklärung der Grafik, siehe gestrichelte Linien. Bei einer Wandoberflächentemperatur von 12°C (linke Seite) soll die relative Luftfeuchte 100 % mit einer absoluten Luftfeuchtigkeit 10 g/m betragen, es kommt somit an Wandoberfläche zur Tauwasserbildung. Geht man von diesem Punkt nach unten, so kann man auf den Kurven die relative Luftfeuchte im Raum ablesen. So liegt z.B. bei 20°C (siehe linke Seite) die relative Luftfeuchte bei 60 %. Um keine Tauwasserbildung an der kalten Wandoberfläche zu erhalten, muss die absolute Luftfeuchte (siehe unten) von 10,3 g/m³ auf 8,5 g/m³ verringert werden. Das entspricht dann bei 20°C einer relativen Luftfeuchte von 50 %. An der Wand beträgt dann die relative Luftfeuchte ca. 80 %. Um die Wandoberfläche schimmelfrei zu halten, müsste die absolute Luftfeuchte weiter abgesenkt werden, oder man erhöht die Oberflächentemperatur.
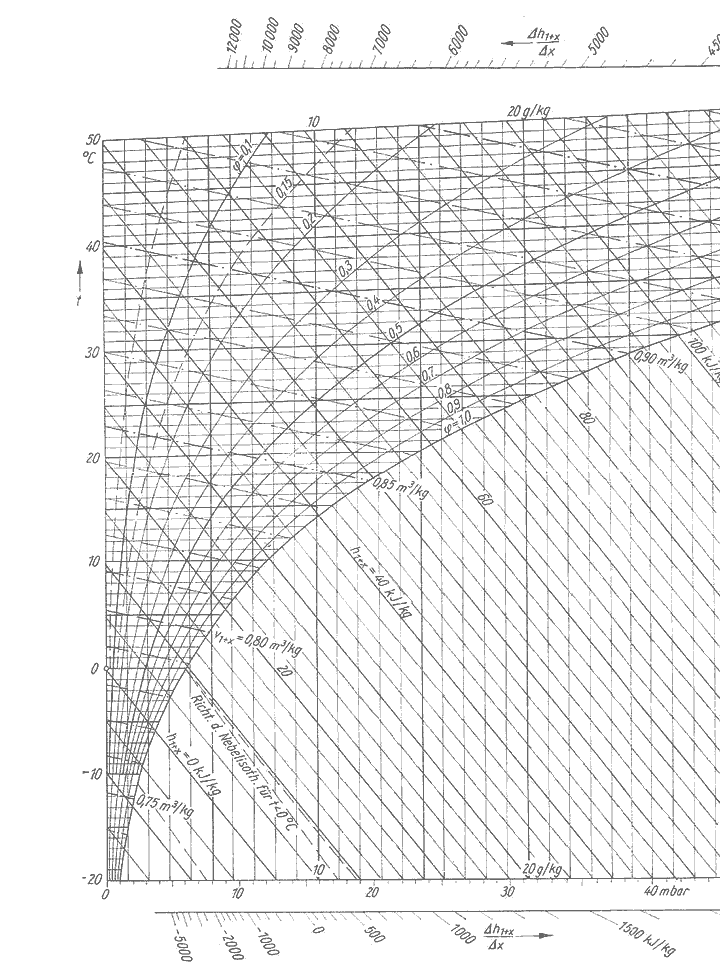
Anlage 5: Teilauszug Mollier-h-x-Diagramm [64]
Anlage 6: Klinisch relevante Schimmelpilze und die verursachten Erkrankungen
Schimmelpilze, die Infektionen über den Luftweg hervorrufen:
| Species | Erkrankung | Risikogruppe nach TRBA 460 |
| Absidia species | Mucorinfektion in Lunge, Nasennebenhöhlen, ZNS, Auge, Haut | 1 |
| Aspergillus fumigatus | Invasive pulmonale Aspergillose; Invasive Aspergillose der Nasen-Nebenhöhlen; Invasive Aspergillose (Infektion von Gefäßen, Leber, Herz, Auge, n. opticus, ZNS, Rückenmark, Haut); Aspergillom (Lunge und Nasennebenhöhlen); Sinusitis; Allergische bronchopulmonale Aspergillose; Otitis externa |
2 |
| Aspergillus nidulans | Invasive Aspergillose | 1 |
| Aspergillus niger |
Invasive Aspergillose sehr selten; Otitis externa; Aspergillose (Lunge und Nasennebenhöhlen) |
1 |
| Aspergillus flavus | Invasive Aspergillose sehr selten; Nasennebenhöhlenaspergillom; Allergische bronchopulmonale Aspergillose |
2 |
| Aspergillus terreus |
Invasive Aspergillose sehr selten; Otitis externa |
1 |
| Cladophialophora bantiana | Hirnabszesse | 3 |
| Conidiobolus species | chronische Nasenschleimhautentzündung | 2 |
| Cunninghamella species | Disseminierte und pulmonale Allgemeininfektionen | 1 |
| Exophiala dermatitidis | Sinusitis, Pneumonie, Hirnabszesse | 2 |
| Fusarium species | Fusariose | 1-2 |
| Mucor species | Infektionen von Nasennebenhöhlen, Lunge, ZNS, Auge, Haut | 1 |
| Paecilomyces variotii | Paecilomykose | 1 |
| Penicillium species | Besiedlung des Bronchialtraktes (Penicillose) | 1-2 |
| Phoma species | Phaeohyphomycose | 1 |
| Pseudoallescheria Boydii | Sinusitis, Pneumonie, Arthritis, Osteomyelitis, Endophthalmitis, Hirnabszesse | 2 |
| Rhizomucor species | Infektionen von Nasennebenhöhlen, Lunge, ZNS, Auge, Haut | 1 |
| Rhizopus species | Infektionen von Nasennebenhöhlen, Lunge, ZNS, Auge, Haut | 1 |
| Ramichloridium mackenzie | Hirnabszesse | 1 |
| Phialophora richardsiae | Zystische Phaeohyphomykose | 1 |
| Syncephalastrum species | Pilzball im Respirationstrakt | 1 |
| Stachybotrys ata (chartarum) | Immunsuppressiv, haemorrhagisch, Pneumonitis |
Hinsichtlich des Auftretens von Infektionen sollten alle Schimmelpilze, die in die Risikogruppe 2 und 3 nach TRBA 460 eingestuft sind, als problematisch angesehen werden. Von großer Bedeutung als wichtigster Mykoseerreger gilt Aspergillus fumigatus. Weiterhin gelten Mykotoxinbildner als problematisch, wenn die Toxine kanzerogen sind. Es werden nicht immer Mykotoxine gebildet, meist sind hohe Keimzahlen erforderlich. Nur bei Stachybotrys chartarum können bereits bei geringer Sporenbelastung in der Raumluft Toxinwirkungen auftreten. [181]
Schimmelpilze in Wohngebäuden ISBN 9783000129469 2007 und Ergänzungen 2021
- Peter Rauch PhD -
Das eBook Schimmelpilze als Downlod kaufen (10 Euro) oder auf Amazon als Kindle eBook 10,00 Euro oder als Taschenbuch (ISBN: 9781078182386) für 23,80 Euro kaufen.
© Bauratgeber | Marktplatz der Bauideen | Sanierungskosten | Bauökonomie | Datenschutzerklärung | Impressum | 01/2021 ![]()

