Es werden in diesem Periodensystem vorwiegend die chemischen Elemente mit einem Link zur ausführlichen Erläuterung versehen, welche als Bestandteil von Baustoffen im Bauwesen Anwendung finden.
Periodisches System: Die Eigenschaften der Elemente ändern sich mit steigender Ordnungszahl (Kernladungszahl) in durch die Elektronenkonfiguration vorgegebenen "Perioden". Das gilt für ihre physikalischen Eigenschaften, für die Art, wie sie Verbindungen mit anderen Elementen eingehen, und auch für die Eigenschaften analoger Verbindungen. Derzeit wurden 114 chemische Elemente bestimmt, von denen einige aber noch nicht sicher nachgewiesen sind. Nur 91 dieser Elemente kommen natürlich vor.
Im Periodensystem der Elemente sind diese Elementgruppen grafisch dargestellt. In den Spalten findet man die Haupt- und Nebengruppen. Die Zeilen entsprechen den 'Perioden', das heißt, den Elektronenschalen, die mit wachsender Ordnungszahl aufgefüllt werden. Die Elemente lassen sich in Metalle und Nichtmetalle aufteilen. Zu den Nichtmetallen gehören auch der Wasserstoff und die Edelgase.
Wichtige Untergruppen sind: Edelgase: Gruppe 0; Alkalimetalle: Hauptgruppe 1 ohne den Wasserstoff); Erdalkalimetalle: Hauptgruppe 2 (ohne Be und Ra); Halogene: Hauptgruppe 7; Eisenmetalle (Fe, Ni, Co), leichte Platinmetalle (Ru; Rh, Pd) und schwere Platinmetalle (Os, Jr. Pt): Gruppe 8.
91 der Elemente kommen natürlich vor, es werden immer weitere Elemente, z. B. 118 Moskowium, entdeckt. Inoffiziell gibt es 143 Elemente im Periodensystem. Diese spielen für das Bauwesen keine Rolle und werden daher auch nicht genannt. (Boris Bolotov entdeckte 5000 Elemente.)
Larson stellt ein besseres Atommodell basierend auf der Physik des Reziproken Systems (RS) vor. Das Konzept geht von skalaren Bewegung aus. Die natürliche Konsequenz dieses Modells beruht darauf, dass für die Atome zwei "Zerstörungslimiten" existieren. Das sind ein Wärmelimit und ein Alterslimit. Das Alterslimit betrifft das Einfangen von geladenen Elektron-Neutrinos durch die Atome, welche isotopische Masse aufbauen. Das Wärmelimit tritt bei thermonuklearen Reaktionen auf. [1]
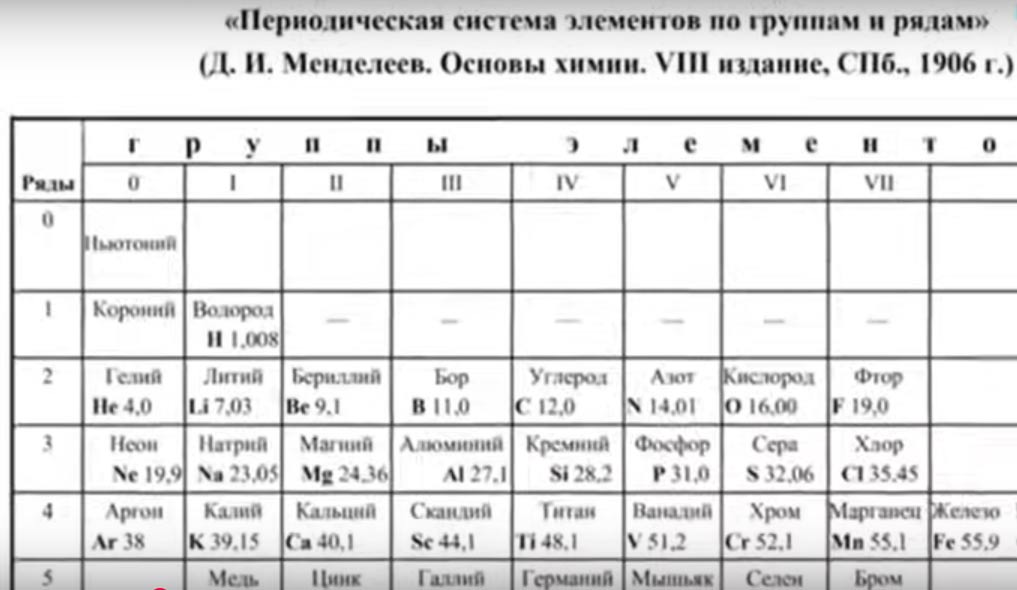
Im Periodensystem von Dmitri Iwanowitsch Mendelejew befand sich das Element x bzw. Äther (Newtonium) im nachfolgendes Bild. Mendelejew hielt es für das leichteste Element. Dieses Element wurde aus dem Periodensystem entfernt und einschließlich verändert, da Kohlenstoff als Hauptenergiequelle dienen sollte. Äther ist eine unerschöpfliche Quelle sauberer Energie und ist nicht erwünscht. Nach der Definition in der Larus Enzyklopädie von 1998 ist Äther eine schwerelose elastische Flüssigkeit, welche den Raum ausfüllt, alle Körper durchdringt und von den Physikern als Ursache von Licht, Wärme, Elektrizität und so weiter anerkannt wurde. (Auf die Tesla Äthertechnologie soll hier nicht eingegangen werden.) [2]
| Periode | I. Hauptgruppe Nebengruppe | VIII. Hauptgruppe Nebengruppe | ||||||||||||||||
1 | 1 1,008
H
|
II. Hauptgruppe Nebengruppe |
III. Hauptgruppe Nebengruppe |
IV. Hauptgruppe Nebengruppe |
V. Hauptgruppe Nebengruppe |
VI. Hauptgruppe Nebengruppe |
VII. Hauptgruppe Nebengruppe |
2 4,003
He
Helium |
||||||||||
2 | 3 6,94
Li
Lidium | 4 9,01
Be
Beryllium | 5 10,81
B
| 6 12,01
C
| 7 14,007
N
| 8 15,999
0
| 9 18,998
F
Fluor | 10 20,18
Ne
Neon |
||||||||||
3 | 11 22,989
Na
Natrium | 3 24,31
Mg
| 13 26,89
AL
| 14 28,09
Si
| 15 30,97
P
Phosphor | 16 32,06
S
| 17 35,45
Cl
| 18 39,95
Ar
Argon | ||||||||||
4 | 19 39,11
K
Kalium | 20 40,08
Ca
Kalzium | 21 44,96
Sc
Skandium |
22 47,90
Ti
|
23 50,94
V
|
24 51,996
Cr
|
22 54,94
Mn
|
26 55,85
Fe
|
27 58,93
Co
|
28 58,71
Ni
|
||||||||
29 63,54
Cu
|
30 65,37
Zn
|
31 69,72
Ga
Gallium | 32 72,59
Ge
Germanium | 33 74,92
As
| 34 78,96
Se
Selen | 35 79,91
Br
Brom | 36 83,80
Kr
Krypton | |||||||||||
5 | 37 85,47
Rb
Rubidium | 38 87,62
Sr
Strontium | 39 88,91
Y
Yttrium |
40 91,22
Zr
Zirkonium |
41 92,91
Nb
|
42 95,94
Mo
|
43 [99]
Tc
Technetium |
44 101,07
Ru
Ruthenium |
45 102,91
Rh
Rhodium |
46 106,4
Pd
Palladium | ||||||||
47 107,87
Ag
|
48 112,40
cd
Kadmium |
49 114,82
In
Indium | 50 118,69
Sn
| 51 121,75
Sb
| 52 127,60
Te
Tellur | 53 126,90
J
Jod | 54 131,30
Xe
Xenon | |||||||||||
6 | 55 132,91
Cs
Zäsium | 56 137,34
Ba
Barium | 57* 138,91
La
Lanthan |
72 178,49
Hf
Hafnium |
73 180,95
Ta
|
74 183,85
W
|
75 186,2
Re
Rhenium |
76 190,2
Os
Osmium |
77 192,2
Ir
Iridium |
78 195,09
Pt
Platin |
||||||||
79 196,97
Au
|
80 200,59
Hg
Quecksilber |
81 204,37
TI
Thallium | 82 207,19
Pb
| 83 208,98
Bi
Wismut | 84 209
Po
Polonium | 85 [210]
At
Astat | 86 [222]
Rn
Radon | |||||||||||
7 | 87 [223]
Fr
Franzium | 88 [226]
Fr
Radium | 89** [227]
Ac
Aktinium |
104 [261]
Ku
Kurtscha-tovium |
||||||||||||||
*Die Lanthanide und die **Aktinide werden hier nicht aufgeführt. Im Periodensystem werden sie mit aufgeführt.
Erläuterung:
|
|
In einer anderen Datei wird ausführlicher der Aufbau des Periodensystems erklärt. Hier sind auch alle Lanthanide und die Aktinide aufgeführt.
© Altbausanierung | Bauideen | gesund Leben | Impressum | AGB/Datenschutzerklärung | 1/2019 ![]()